Что такое прогрессирующая оссифицирующая фибродисплазия?
Термин «фибродисплазия прогрессирующая оссификанс» уже указывает на прогрессирующий рост кости. Это происходит скачкообразно, при этом новые кости могут образовываться из мышечной или соединительной ткани даже при малейшей травме. Нарастающую оссификацию остановить невозможно.
При медикаментозном лечении возможно только частичное замедление роста костей. Следует избегать хирургических вмешательств или инфузий в мышцу, так как они могут вызвать новую вспышку окостенения. Впервые болезнь была упомянута в 1692 году французским врачом Ги Патеном. В 1869 году врач Эрнст Мюнхмайер описал синдром, который тогда еще называли Синдром Мюнхмейера был обозначен.
Другие названия фибродисплазии ossificans progressiva (ФОП) в дополнение к синдрому Мюнхмейера среди других Оссифицирующая множественная прогрессирующая фибродисплазия или Прогрессирующий оссифицирующий миозит, ФОП является генетическим. Их частота – 1 из 2 миллионов.
Крайняя редкость заболевания объясняется тем, что это аутосомно-доминантная мутация. Человек, пораженный ФОП, обычно не имеет потомства. Следовательно, это почти всегда новые мутации. В настоящее время известно, что около 600 человек во всем мире страдают прогрессирующей оссифицирующей фибродисплазией.
Симптомы ОПФ
У рожденных с ОПФ, признаки и симптомы окостенения могут никак не выявляться, пока ребенок не станет немного старше и не начнет расти.
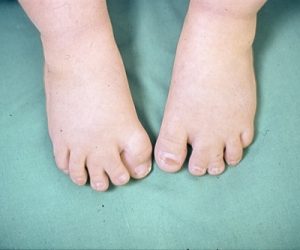
У новорожденных первым признаком ОПФ часто является врожденная аномалия пальцев ног.
Вскоре после рождения медицинские работники или родители могут заметить, что большие пальцы ноги ребенка короче других пальцев (см. фото выше).
Этот порок развития наблюдается у всех людей с синдромом каменного человека и является важной подсказкой для постановки диагноза. У новорожденного также могут быть отеки вокруг глаз и кожи головы
В некоторых случаях этот отек может начаться, когда плод еще находится в утробе матери, хотя это состояние обычно диагностируется только после рождения. Около 50 процентов людей с этим заболеванием также имеют сходные врожденные аномалии в больших пальцах — также наблюдались и другие пороки развития, например, в позвоночнике
У новорожденного также могут быть отеки вокруг глаз и кожи головы. В некоторых случаях этот отек может начаться, когда плод еще находится в утробе матери, хотя это состояние обычно диагностируется только после рождения. Около 50 процентов людей с этим заболеванием также имеют сходные врожденные аномалии в больших пальцах — также наблюдались и другие пороки развития, например, в позвоночнике.
Большинство людей с оссифицирующей прогрессирующей фибродисплазией впервые испытывают основные симптомы заболевания (иногда их называют «обострениями») к 10 годам жизни.
Однако, поскольку на формирование кости могут повлиять травма (например, перелом руки) или вирусное заболевание (например, грипп), заболевание может не строго следовать этому прогрессу.
Основные симптомы болезни Мюнхеймера зависят от того, какие части тела стали окостеневшими. Часто, при заболевании встречаются нежные комки под кожей (подкожные узелки, см. фото выше). Иногда формированию этих узелков предшествует умеренная лихорадка. Большинство людей с ОПФ будут иметь общие симптомы боли, ригидности и прогрессирующего недостатка подвижности по мере разрастания костной ткани.
В зависимости от того, какие части тела окостенеют, более специфические симптомы ОПФ могут включать:
- проблемы с питанием, которые могут привести к дефициту питательных веществ или недоеданию;
- трудно с разговором;
- проблемы с зубами;
- затрудненное дыхание;
- респираторные инфекции;
- нарушение слуха;
- выпадение волос (облысение);
- анемию;
- сдавливание нервов;
- правосторонняя застойная сердечная недостаточность;
- искривление позвоночника (сколиоз и кифоз).
- сенсорные аномалии;
- умеренную умственную отсталость;
- неврологические симптомы.
Лечение оссифицирующей прогрессирующей фибродисплазии
Современная медицина еще не изобрела лекарство, которое лечило бы фибродисплазию. Но и методы по облегчению состояния больного значительных результатов не приносят. При первых проявлениях заболевания положительная динамика наблюдается во время использования глюкокортикостероидов, тем самым уменьшая проявления болезни и улучшая качество жизни пациента, но к полному выздоровлению не приводит. Полностью избавиться от костных наростов при помощи глюкокортикостероидов не представляется возможным.
Период обострения болезни начинается очень резко, даже спонтанно, и также неожиданно заканчивается, оставляя за собой костное образование. В современном мире тратится очень большое количество времени и средств на изучение данной патологии, целью данных исследований является улучшение качество жизни и состояния здоровья таких пациентов. Было проведено исследование на лабораторных мышах, при использовании лекарственного препарата было установлено, что он помогает бороться с признаками фибродисплазия вызванной как мутировавшим геном, так и травмами. На людях, к сожалению, эти испытания не проводились, потому что невозможно найти достаточное количество пациентов с фибродисплазией для проведения клинических испытаний. В виду отсутствия пациентов, данный лекарственный препарат будет находиться на стадии разработки еще длительное время. Но в 2014 вроде удалось собрать необходимое количество пациентов для клинических испытаний лекарственного препарата «Паловаротен», испытания проводятся сразу в нескольких городах – Париж, Филадельфия и Сан-Франциско.
Среди клиник по лечению оссифицирующей прогрессирующей фибродисплазии самой лучшей считается лаборатория Маккея при Пенсильванском Федеральном Университете, которой руководит доктор медицинских наук Фредерик Каплан. Это единственная в мире лаборатория, которая специализируется на изучение феномена фибродисплазии. В России также можно провести диагностические процедуры относительно фибродисплазии, которые проводятся в медико-генетическом научном центре РАМН в Москве по ул. Москворечье д. 1. В НИИ Ревматологии профессор Никишина И.П. и в ММА имени Сеченова профессор Голованова Н.Ю. (Москва) проводят терапевтическое лечение, а также в Иркутском государственном медицинском университете доктор медицинских наук Калягин А.Н. (Иркутск) и в Казанской Государственной Медицинской Академии доктор медицинских наук Мальцев С.В. (Казань).
Методы лечения
На ранних стадиях развития болезни назначают медикаментозное лечение.
На начальных стадиях болезни применяют глюкокортикостероиды, которые уменьшают разрушительное воздействие недуга на организм и облегчают процессы жизнедеятельности больных. К полному выздоровлению прием данных лекарств привести не может. Существуют медикаментозные средства, способные затормозить развитие болезни. Среди прочих препаратов можно выделить «Интерферон-g», длительное применение которого способствует уменьшению мышечных уплотнений. Кроме того, больным показаны к применению биофосфонаты и этилендиаминтетрауксусная кислота.
Новый препарат «Паловаротен» применяют для блокирования очагов разрастания костной ткани. А «Интерферон лейкоцитарный» при длительном применении, способен снизить количество костных образований. Своевременная диагностика позволит вовремя распознать болезнь и начать лечение глюкокортикостероидами, что продлит жизнь пациента и улучшит ее качество.
Признаки и симптомы
Независимо от формы оссифицирующего миозита, основным его симптомом является боль в пораженной мышце. Болезненные ощущения нередко сопровождаются мышечной скованностью, напряжением, снижением подвижности суставов. При осмотре выявляется болезненность, которая усиливается во время пальпации и растяжения. Если оссификация сопровождается воспалительным процессом, в месте воспаления могут определяться узелки и мышечные тяжи (уплотнения, возникающие при интенсивных спазмах мышечного волокна).
Другими клиническими симптомами также являются:
- инфильтрация мягких тканей;
- изменение оттенка кожи в области пораженного участка;
- усиление болей во время движения, а также в состоянии длительного покоя (например, во время ночного сна);
- уплотнение и отечность тканей;
- утолщение кожного покрова в месте локализации оссифицированной мышцы;
- ограничение пассивной подвижности и деформация суставов в зоне иннервации пораженной мышцы.
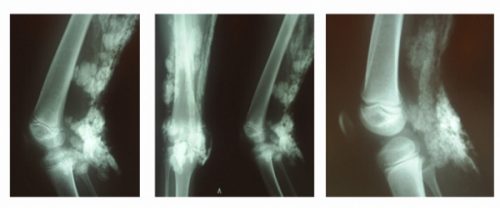
Внешний вид и рентгенограмма пациента с миозитом
Перечисленные симптомы характерны для острой травматической формы оссифицирующего миозита. Трофоневротическая и прогрессирующая разновидность заболевания имеют свои особенности, позволяющие качественно проводить первичную диагностику и своевременно выявлять возможные отклонения.
Типичные и характерные особенности
Отличительные особенности каждой разновидности оссифицирующего миозита перечислены в таблице ниже.
Симптомы оссифицирующего миозита
| Форма заболевания | Клиническая картина |
|---|---|
| Травматическая (посттравматическая) | Симптомы патологического процесса в мышечной ткани в большинстве случаев выражены слабо. У части больных первые мышечные боли, ассоциированные с оссификацией мышц, могут появиться только спустя несколько месяцев после получения травмы, поэтому ранняя диагностика травматического оссифицирующего миозита возможна лишь в исключительных случаях.
Боли при посттравматической оссификации мышц чаще всего умеренные (пациенты обращаются за медицинской помощью после появления болезненного подкожного уплотнения) |
| Фибродисплазия (прогрессирующий фибромиозит) | Под кожей появляются припухлости, кожа вокруг которых может быть отечной и гиперемированной. Со временем припухлости становятся менее выраженными, а на их месте возникают болезненные уплотнения. Стремительно нарастает мышечная слабость (миастения) и атрофия мышечного волокна. Меняется походка человека, его мимика. При шейном прогрессирующем оссифицирующем миозите возможно нарушение дыхательной и глотательной функции (в тяжелых случаях – асфиксия дыхательных путей) |
| Параартикулярная (трофоневротическая) | Клиника параартикулярного окостенения схожа с симптомами фибродисплазии, но в зоне уплотнений также появляется гипертермия. Кожный покров становится горячим, теряет свою подвижность, покрывается венозным рисунком. Одним из явных признаков является патологическое снижение пассивной подвижности иннервируемых суставов |
Лечение и терапия
Прогрессирующую оссифицирующую фибродисплазию пока нельзя лечить причинно. Возможно только симптоматическое лечение. Течение болезни не остановить, а хотя бы отсрочить медикаментозным лечением
В медикаментозной терапии основное внимание уделяется лечению боли в случае приступа.
Используются противовоспалительные препараты, такие как кортикостероиды и нестероидные противовоспалительные препараты. Исследования все еще продолжаются в отношении варианта причинной терапии с использованием антител и ингибиторов передачи сигнала против рецептора ACVR1. Однако эта терапия еще не готова к применению. Однако нельзя удалять дополнительные кости хирургическим путем, так как это приведет к новому обострению болезни с гораздо более сильным окостенением.
Стадии
Заболевание фибродисплазия развивается постепенно и имеет несколько стадий прогрессирования, таких как:
- возникновение небольшого свойственного одному месту воспаления;
- распространение недуга на соседние здоровые ткани и увеличение площади воспалительного процесса;
- появление бессосудистого уплотнения;
- образование плотной и упругой соединительной ткани;
- этап формирования остеогенеза и окостенения.
Особенности проявления недуга во многом зависят от стадии развития, возрастной категории и влияния на организм человека сопутствующих факторов из вне.
По окончании периода обострения в течении некоторого времени при отсутствии каких-либо травм заболевание может не напоминать о себе совсем. Но такие случаи бывают крайне редко. В основном недуг переходит сразу к активному прогрессированию и человек становится все менее и менее подвижным, а со временем инвалидом. Поначалу возникает ограничение движений в крупных суставах – плечевых, локтевых, коленных, тазобедренных.
Затем поражению поддаются более мелкие суставы и хрящи, которые являются соединительным звеном между рёбрами и позвоночным столбом. Момент, в который будет происходить пиковое обострение фибродисплазии, нельзя предвидеть в связи с тем, что стартом для развития недуга является наша иммунная система. Все составляющие мышечного аппарата подвержены процессу импрегнации хрящевой и соединительной ткани в костную.
Исследовать
Клинические испытания изотретиноина , этидроната с пероральными кортикостероидами и пергексилина малеата не продемонстрировали эффективности, хотя вариабельность течения заболевания и небольшая распространенность вызывают неопределенность.
Несколько фармацевтических компаний, специализирующихся на редких заболеваниях, в настоящее время находятся на разных стадиях исследования различных терапевтических подходов к ФОП.
В августе 2015 года Управление по разработке орфанных продуктов Управления по санитарному надзору за качеством пищевых продуктов и медикаментов США (FDA) предоставило La Jolla Pharmaceuticals статус орфанных лекарств для двух новых соединений для FOP. Эти соединения представляют собой низкомолекулярные ингибиторы протеинкиназы, разработанные для селективного блокирования ACVR1 (ALK2).
В августе 2015 года Clementia Pharmaceuticals также начала набор детей (в возрасте 6 лет и старше) в свое клиническое испытание фазы II, посвященное изучению паловаротена для лечения ФОП. Доклинические исследования показали, что паловаротен, гамма-агонист рецепторов ретиноевой кислоты, блокирует аномальное образование костей в моделях на животных путем ингибирования систем вторичных мессенджеров в пути BMP. Clementia получила лицензию на паловаротин от Roche Pharmaceuticals, которая ранее оценила это соединение более чем на 800 людях, включая здоровых добровольцев и пациентов с хронической обструктивной болезнью легких. Паловаротен получил обозначение Fast Track от FDA и обозначение сирот для лечения FOP как от FDA, так и от Европейского агентства по лекарственным средствам (EMA).
В сентябре 2015 года Regeneron объявила о новом понимании механизма заболевания, связанного с активацией рецептора ACVR1 активином A. В 2016 году компания начала исследование фазы 1 своего антитела к активину, REGN 2477, на здоровых добровольцах; в 2017 г. было проведено исследование фазы 2 у пациентов с ФОП.
Другой потенциальный терапевтический подход включает интерференцию аллель-специфической РНК, которая нацелена на деградацию мутированной мРНК при сохранении нормальной экспрессии гена ACVR1.
Дальнейшие исследования механизмов образования гетеротопической кости при ФОП могут помочь в разработке методов лечения других заболеваний, связанных с формированием внескелетной кости.
Фибро / адипогенные предшественники (FAP) могут быть типом клеток, вызывающих заболевание, ответственных за зависимое от активина A образование эктопической кости как в мышцах, так и в сухожилиях мышей, несущих FOP, вызывающую мутацию ACVR1 (R206H).
По состоянию на 2019 год продолжаются клинические испытания нескольких потенциальных методов лечения.
Клиники для лечения фиброзной дисплазии
Так как фиброзная дисплазия – это очень редкое заболевание, обратиться за лечением лучше в узкопрофильные клиники. Большой опыт врачей способствует точной диагностике болезни на ранних этапах. Кроме того, в зарубежных центрах ТОП-уровня есть возможность проводить операции на костях минимально инвазивным методом. Такие вмешательства облегчают период реабилитации для пациентов и оставляют меньшие шрамы.
В приоритете находятся клиники с сильными отделениями онкологии, ортопедии, педиатрии, хирургии, неврологии
Резюме
Фиброзная дисплазия – это редкое доброкачественное заболевание костей, вследствие которого повышается их хрупкость. Эта болезнь чаще всего диагностируется в детском возрасте, но остается на всю жизнь. Чаще всего поражены бедренная, большеберцовая и малоберцовая кости. Несколько реже встречается фиброзная дисплазия костей черепа, таза, позвоночника или ребра.
Диагностика фиброзной дисплазии включает рентген, КТ, МРТ, остеосцинтиграфию, биопсию и генетический анализ крови.
В большинстве случаев если болезнь не вызывает никаких симптомов, можно обойтись без какого-либо вмешательства. Лечение фиброзной дисплазии, зависимо от размера и расположения опухоли, включает медикаментозные препараты, операцию и физиотерапию.
Среди ведущих клиник, в которых проводят лечение фиброзной дисплазии, медицинские центры Турции, Израиля, Германии, Австрии, Испании, Польши и Чехии.
Симптоматика
Фибродисплазия не сразу после рождения проявляет себя: первые симптомы можно заметить у ребенка в возрасте от нескольких месяцев до нескольких лет.
Существуют два ярко выраженных симптома болезни Мюнхеймера:
- появление в волокнах воспалительных нарушений;
- гетеротопическое костеобразование.
Также симптоматика может отображать аномалии развития человека или окостенения тканей, например:
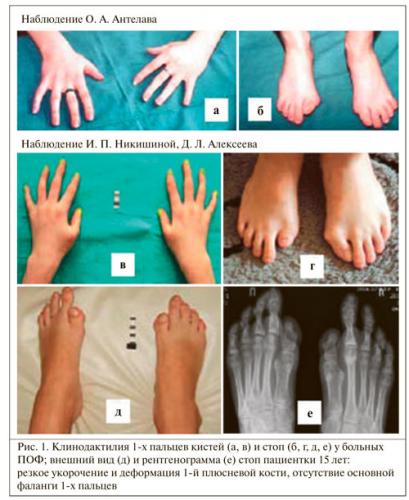
- короткий первый палец стопы;
- клинодактилия – отсутствие сустава первого пальца стопы, его изогнутость вовнутрь;
- гипоплазия фаланги, короткие большие пальцы на кистях;
- искривленность пятого пальца;
- отек мягкой ткани головы от минимального повреждения (небольшой ушиб, царапина);
- нарушения в строении позвоночника шейного отдела;
- наличие более широких и коротких костей плеча и бедра;
- не исключается задержка психического развития, глухота, облысение.
Такие заболевания, как сколиоз, кривошея – частое явление при прогрессирующей оссифицирующей фибродисплазии.
Лечение
Огромное количество учёных работает над изучением фибродисплазии и изобретением медицинских препаратов и других способов лечения, которые помогут справиться с болезнью и остановить её распространение по всему организму. На сегодня нет таких лекарств и способов, способных излечить больного от недуга.
На начальных стадиях облегчение может принести приём глюкокортекостероидов. Медикаменты, принадлежащие к данной группе, способствуют уменьшению проявления фибродисплазии и тем самым улучшают качество жизни, но, к сожалению, не приводят к полному устранению патологии.
Также используют биофосфонаты и биостимуляторы, которые помогают уменьшить количество мигрирующих остеобластов, улучшая при этом процессы обмена в организме. Периоды активного развития новых уплотнений происходят внезапно и также спонтанно заканчиваются уже полноценным костным образованием.
Помимо медикаментозного способа есть также хирургический, который заключается в оперативном удалении возникших очагов окостенения. После проведения нескольких операций было выявлено, что в результате хирургического вмешательства происходит усиление оссификации. В связи с этим данный метод не имеет эффективности.
Поскольку данный недуг является очень редким, учёные не могут собрать необходимое количество пациентов для проведения нужных исследований, которые в дальнейшем помогут улучшить качество жизни людям, страдающим от фибродисплазии.
На первых этапах прогрессирования болезни можно применять физиотерапию, а точнее электрофорез с йодидом калия. Пациентам не рекомендуется применять массаж, парафинотерапии и УВЧ.
Симптомы
Оссифицирующая фибродисплазия редко начинает развиваться сразу же после рождения ребенка
Врачи обращают внимание на нарушение сформированности пальчиков на ногах и руках. Никаких других внешних проявлений не наблюдается
Оссификация начинается внезапно, порой без наличия объективной причины. Возраст ребенка может быть от 2-3 месяцев до нескольких лет. Чаще прогрессирование происходит в первые пять лет жизни. Симптомами заболевания считаются:
- Ранняя симптоматика проявляется формированием небольшого уплотнения, размером до 3 мм,
- При прогрессировании уплотнение увеличивается до 10 см,
- При пальпации наблюдается болезненность, иногда покраснение,
- Походка у пациента приобретает неуверенность, скованность,
- На лице отсутствуют какие-либо эмоции,
- Происходит уменьшение объема движений, что имеет связь с появлением новых уплотнений, приводя к полной обездвиженности,
- При прощупывании появляются боли в ногах,
- Нарушается чувствительность,
- Происходят сбои функционирования внутренних органов.
Наиболее очевидной клинической картиной заболевания считают окостенение мягкой ткани. Но возможно проявление следующих дефектов, говорящих о наличии оссифицирующей фибродисплазии:
- Короткий по отношении к остальным большой палец ноги, характеризующийся изогнутостью внутрь,
- Дефект в шейном отделе позвоночника,
- Короткий большой палец рук,
- Отставание в развитии,
- Глухота,
- Облысение,
- Искривление пятого пальца ног,
- Кривошея,
- Сколиоз,
- Тугая подвижность костного сочленения.
Известны случаи, когда уплотнения самостоятельно рассасываются, но в последствии образуются снова. После чего через 2-3 недели происходит их окостенение, в результате которого стает невозможным дальнейшее их рассасывание. У взрослого пациента прогрессирующая болезнь Мюнхеймера приводит к слиянию десятков очагов. Что в последствии вызывает глубокую инвалидизацию и летальный исход.
Симптомы заболевания
Характерными признаками ФОП считаются воспалительные процессы в мягких тканях и гетеротопическая оссификация. Вновь образующиеся кости практически не отличаются от уже имеющихся. Окостенение мягких тканей способствует развитию мышечной слабости, дистрофических нарушений и сращения суставов. Не выявлено факторов, под воздействием которых окостенение приобретает локальный характер либо распространяется по всему организму.
Симптомы ФОП представляют собой не только оссификацию мягких тканей, но и различные аномалии развития. Наиболее распространенными являются:
- короткопалость стоп;
- гипоплазия фаланг кистей;
- клинодактилия пятого пальца; и
- скривление шейного отдела позвоночника, которое можно увидеть на фото;
- укорочение и расширение плечевых и бедренных костей.
Существует высокий риск развития тугоухости, аллопеции, гипогонадизма и отставания в физическом развитии. Практически у всех пациентов обнаруживаются признаки кривошеи, сколиоза и снижения подвижности суставов.
В настоящее время наиболее важную роль играют генетические исследования. Основной находкой в этой области считается обнаружение мутации BMP4-гена и его РНК у 70% пациентов. ВМР-4 — белковое соединение, ответственное за формирование костных тканей и заживление переломов. Оно содержит гены, повреждение которых может привести к развитию фибродисплазии.